Modelos atómicos
La evolución del átomo comenzó desde el siglo V a.C., por Empédocles que decía que toda la materia estaba formada por los 4 elementos: aire, agua, tierra y fuego.
Aproximadamente 400 años antes de Cristo, el filósofo griego Demócrito consideró que la materia estaba constituida por pequeñísimas partículas que no podían ser divididas en otras más pequeñas. Por ello, llamó a estas partículas átomos, que en griego quiere decir "indivisible". Demócrito atribuyó a los átomos las cualidades de ser eternos, inmutables e indivisibles.
Cerca de 2200 años después, la idea de átomo fue retomada por Dalton e inicio un proceso de evolución, hasta la actual teoría cuántica.

Modelo Atómico de Thomson

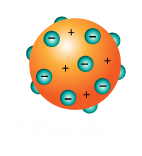
En 1904, Joseph John Thomson propone el primer modelo atómico con las siguientes características:
• El átomo es de forma esférica, compacta y con carga positiva, distribuida homogéneamente; en la cual, se encuentran incrustados los electrones, con un movimiento vibratorio y en cantidad suficiente como para neutralizar la carga positiva de la esfera; por lo tanto, el átomo es eléctricamente neutro.
• Por la apariencia que presentaba este modelo, fue denominado: “Modelo Budin de Pasas”.
Modelo Atómico de Dalton

John Dalton, en el año 1808, enunció los siguientes postulados:
• La materia está formada por partículas pequeñísimas llamadas “átomos”.
• Estos átomos no se pueden dividir, no se crean ni se destruyen, y nunca cambian.
• Los átomos de un mismo elemento son iguales entre sí, tienen la misma masa y dimensiones.
• Los átomos de elementos diferentes, son diferentes; por ejemplo, los átomos de oxígeno son diferentes a los átomos de hidrógeno.
• Los átomos, al combinarse para formar compuestos guardan relaciones simples.
• Los átomos de elementos diferentes se pueden combinar en proporciones distintas y formar más de un compuesto.
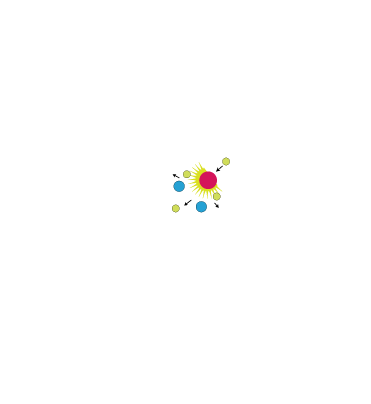
Modelo Atómico de Jean Perrin

Jean-Baptiste Perrin modifico el modelo de Thomson sugiriendo por primera vez que las cargas negativas son externas al “budín”.
En 1895, encontró que los rayos catódicos depositaban carga en un electroscopio, con lo que confirmó que se trataban de partículas cargadas. Fue por aquellas fechas que el inglés Joseph John Thomson se interesó en medir la velocidad de dichas partículas, que serían finalmente identificadas como los electrones.
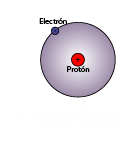
Modelo Atómico de Rutherford (1911)
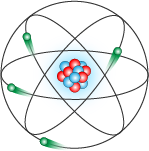
Según Rutherford, el átomo es un sistema dinámico, con un núcleo de carga positiva y los electrones girando alrededor, siguiendo trayectorias circulares y concéntricas a una gran velocidad, de tal modo que se neutralice la fuerza de atracción eléctrica que ejerce el núcleo; por lo tanto los electrones estarían girando alrededor en estado de equilibrio.
Modelo Atómico de Niels Bohr
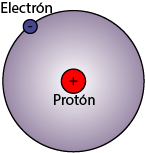
En el año de 1913, Niels Bohr propuso un modelo atómico, fundamentándose en la teoría cuántica de Max Planck y se basó en los siguientes postulados:
• Los electrones se mueven alrededor del núcleo describiendo una órbita circular, en la que el electrón se encuentra en estado estacionario.
• De entre todas las orbitas posibles, el electrón solo puede recorrer aquellas en las que el momento angular del electrón es múltiplo entero de h/2π.
• El paso de un electrón de una órbita a otra implica una transferencia de energía que tiene lugar en forma de radiación electromagnética.
• Cuando los electrones absorben o desprenden energía, lo hacen en cantidades unitarias llamadas cuantos.
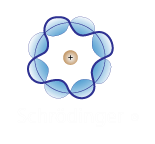
Modelo Atómico de Sommerfeld
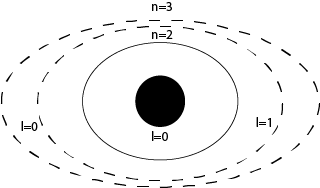
En el año de 1916, Arnold Sommerfeld, realizó modificaciones al modelo de Bohr, al considerar la posibilidad de que el electrón girara alrededor del núcleo en orbitas elípticas, de las que la órbita circular sería un caso particular
• Los electrones se mueven alrededor del núcleo en orbitas circulares.
• A partir del segundo nivel energético existen 2 o más subniveles.
• El electrón es una corriente eléctrica minúscula.
• Introdujo el número azimutal, al cual designo con la letra "l".
Modelo Atómico de Schrödinger

El modelo atómico de Schrödinger desarrolló un nuevo modelo de átomo a través de una ecuación matemática (ecuación de onda) considerando su comportamiento dual. Este comportamiento de onda partícula lleva consigo la imposibilidad (principio de incertidumbre de Heisenberg) de conocer simultáneamente la energía y la posición exacta de un electrón. Schrödinger determinó con exactitud la energía y la posición de un electrón en unas zonas de probabilidad, a las que llama orbitales atómicos.
La caracterización del electrón, en cuanto a su energía, ubicación, giro en torno a su eje, son soluciones de la ecuación de onda, que originaron los cuatro números cuánticos.
Modelo Atómico de Jordan-Dirac
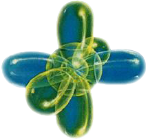
En 1928 Dirac logro una descripción cuanti-relativista del electrón, prediciendo la existencia de la antimateria. En las ecuaciones de Dirac y Jordan aparece el cuarto parámetro con característica cuántica, denominado s, además de los ya conocidos n, l, y m.
En su teoría postularon:
• Además del movimiento alrededor del núcleo, los electrones tienen también un movimiento de rotación sobre sí mismos. Este movimiento denominado de Spin puede ser en sentido del horario.
• Dos electrones que se encuentren en un mismo orbital, poseen siempre un movimiento de spin contrario.