QUÍMICA
Aspectos analíticos de sustancias
Componente:
-
Introducción
-
El Átomo
-
Modelos
atómicos
-
Configuración
Electrónica
-
La materia y
sus propiedades
-
Unidades
de medida
-
Webgrafía
La materia y sus propiedades
La materia, es todo lo que conforma el universo físico, ocupando un lugar en el espacio. Todos los cuerpos están integrados por materia, difiriendo en ellos, su tamaño, su forma y peso. La materia puede presentarse de distintas maneras o estados. Además dependiendo de las condiciones, los cuerpos pueden cambiar su estado o la forma en que se nos presentan.

Propiedades
Generales
Propiedades
Específicas
Masa
Densidad
Conductividad
Punto de ebullición
Punto de fusión
Peso
Volumen
Inercia
Propiedades Generales
Son las propiedades que presenta todo cuerpo material sin excepción y al margen de su estado físico, dependen de la cantidad de materia presente.
Propiedades Específicas
Las propiedades específicas de la materia son aquellas que caracterizan a cada sustancia y permiten diferenciar un objeto o cuerpo de otro.
Masa
La masa es la propiedad que nos permite determinar la cantidad de materia que posee un cuerpo. La masa está relacionada proporcionalmente con el peso, es decir, a mayor masa, mayor es el peso del cuerpo.
La masa de los cuerpos se mide con la balanza y se expresa en kilogramos (Kg), y demás múltiplos y submúltiplos.

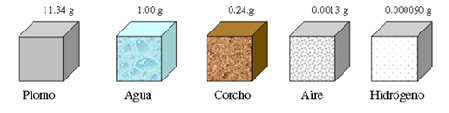
Densidad
La densidad es una medida de cuánto material se encuentra comprimido en un espacio determinado; indica la cantidad de masa por unidad de volumen; mientras mayor sea la cantidad de materia contenida en una unidad de volumen, mayor será la densidad de esa sustancia y viceversa.
![]()
Conductividad
La Conductividad eléctrica, es la capacidad de un cuerpo o medio, para conducir la corriente eléctrica, los iones cargados positiva y negativamente son los que conducen la corriente, y la cantidad conducida dependerá del número de iones presentes y de su movilidad.

Punto de Ebullición
El punto de ebullición, es la temperatura a la cual una sustancia, cambia de la fase líquida a la gaseosa. En el caso de sustancias puras a una presión fija, el proceso de ebullición ocurre a una sola temperatura; al añadir calor la temperatura permanece constante hasta que todo el líquido se ha evaporado.
Punto de Fusión
El punto de fusión, es la temperatura a la cual un sólido cambia a líquido. En las sustancias puras, el proceso de fusión ocurre a una sola temperatura y el aumento de temperatura por la adición de calor se detiene hasta que la fusión es completa.
Peso
El peso es la acción de la gravedad de la Tierra sobre los cuerpos. En los lugares donde la fuerza de gravedad es menor, por ejemplo, en una montaña o en la Luna, el peso de los cuerpos disminuye.
El peso se mide con el dinamómetro y se expresa en Newton (N= kg.m/s2)

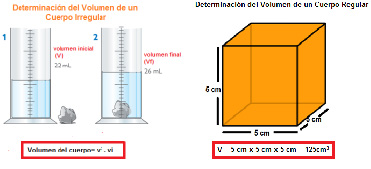
Volumen
El volumen de un cuerpo está determinado por el lugar o espacio que ocupa. Existen cuerpos de muy diversos tamaños. Para expresar el volumen de un cuerpo se utiliza el metro cúbico (m³) y demás múltiplos y submúltiplos.
Inercia
Es una propiedad por la que todos los cuerpos tienden a mantenerse en su estado de reposo o movimiento, todo cuerpo se mantiene en dicho estado, mientras no exista una causa (fuerza) que lo modifique.
x
Webgrafía
x







La materia
La materia, es todo lo que conforma el universo físico, ocupando un lugar en el espacio. Todos los cuerpos están integrados por materia, difiriendo en ellos, su tamaño, su forma y peso
Propiedades
Las propiedades de la materia, son las diversas formas en que impresionan los cuerpos materiales, a nuestros sentidos o a los instrumentos de medida.
Propiedades generales:
Son aquellas que poseen todos los tipos de materia, sin importar las sustancias que la constituyan o el lugar en el que se encuentren, por lo que no nos permiten diferenciar los distintos tipos de sustancias.
Ejemplo: La masa y el volumen.
Propiedades específicas
Son las propiedades particulares que caracterizan a cada sustancia, permiten su diferenciación con otra y su identificación.
Las propiedades específicas pueden ser químicas o físicas dependiendo si se manifiestan con o sin alteración en su composición interna o molecular.
Entre estas propiedades tenemos: La ↔densidad y el punto de ebullición.
Físicos
Son los cambios que sufre la materia en su forma, su volumen o estado, sin alterar su composición o naturaleza.
Ejemplo: Si se calienta un bloque de hielo a determinada temperatura, este se licua, es decir, pasa al estado sólido al líquido modificando su forma y volumen pero conservando su naturaleza.
Químicos
Se manifiestan cuando las sustancias que intervienen presentan cambios en su constitución. Las transformaciones o cambios químicos se denominan reacciones químicas, donde por una redistribución de los átomos, una o varias sustancias (reactivos) se transforman en otra sustancias (producto de la reacción).
Reacciones Químicas
Una reacción química, es todo proceso termodinámico en el cual una o más sustancias (llamadas reactantes), por efecto de un factor energético, se transforman, cambiando su estructura molecular y sus enlaces, en otras sustancias llamadas productos. Las reacciones químicas pueden ser reversibles o irreversibles.
Reversibles
Las reacciones reversibles, son aquellas que ocurren simultáneamente en los dos sentidos, es decir, al mismo tiempo los reactivos se transforman en productos y los productos se transforman en reactivos, el proceso reversible se puede invertir y dejar en las mismas condiciones iniciales al sistema involucrado.
Ejemplo:
N2 : Nitrógeno (gaseoso)
H2 : Hidrógeno (gaseoso)
NH3 : Amoníaco (gaseoso)
N2 + H2 ↔ NH3
Cinética química
La cinética química es el estudio de la velocidad de las reacciones. Pero, además, estudia y desarrolla modelos de los “mecanismos” de dichas reacciones para poder “explicar” los resultados experimentales de las mediciones de dichas velocidades. La velocidad de una reacción depende de la naturaleza de las sustancias, la temperatura, la concentración de los reactivos y la presencia o ausencia de catalizadores.
Concentración de los reactivos.
Se puede comprobar científicamente que la velocidad crece cuando lo hacen las concentraciones de las especies reaccionantes.
Estado físico:
El estado físico de los reactivos condiciona la velocidad de las reacciones. Bastantes reacciones tienen lugar en estado gaseoso preferentemente, o también en disolución, pues así las moléculas poseen mayor libertad de movimiento y se ponen de manera más sencilla en contacto con otras.
La temperatura
La temperatura condiciona un aumento en la velocidad de la reacción. Cuando las temperaturas están próximas a la temperatura que hay en el ambiente, un aumento de 10ºC multiplicaría la velocidad de la reacción por dos.
Catalizadores.
La velocidad de las reacciones químicas, se puede ver modificada cuando existe la presencia de catalizadores. Un catalizador, es una sustancia que aumenta la velocidad de una reacción química, participando en la misma reacción pero sin consumirse.
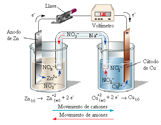
Celdas galvánicas
Las celdas galvánicas funcionan espontáneamente, utilizando una reacción química para realizar trabajo eléctrico. Los electrones se mueven a través del circuito externo desde el lugar de la oxidación (ánodo) hacia el sitio de la reducción (cátodo)
Celdas electrolíticas
Son un dispositivo experimental con capacidad de generar electricidad por medio de una reacción redox (reducción-oxidación) espontánea.
Distribución electrónica
La distribución electrónica consiste en distribuir los electrones en torno al núcleo en diferentes estados energéticos (niveles, subniveles y orbitales).
Tabla periódica
La tabla periódica clasifica, organiza y distribuye de forma correcta todos los elementos químicos, de acuerdo a sus propiedades y características. Su función principal es establecer un orden específico agrupando elementos.
Elementos
Un elemento químico es un tipo de materia constituida por átomos de la misma clase, se identifican con símbolos químicos.
Ejemplo: Oxígeno (O), Nitrógeno (N)
Gaseoso
Los gases, igual que los líquidos, no tienen forma fija pero, a diferencia de éstos, su volumen tampoco es fijo. También son fluidos, como los líquidos.
En un gas el número de partículas por unidad de volumen es también muy pequeño. Las partículas se mueven de forma desordenada, con choques entre ellas y con las paredes del recipiente que los contiene.
Líquido
Los líquidos, al igual que los sólidos, tienen volumen constante, no tienen forma fija y adoptan la forma del recipiente que los contiene. En los líquidos las partículas están unidas por unas fuerzas de atracción menores que en los sólidos, por esta razón las partículas de un líquido pueden trasladarse con libertad.

Solido
Los sólidos se caracterizan por tener forma y volumen constantes. Esto se debe a que las partículas que los forman están unidas por unas fuerzas de atracción grandes de modo que ocupan posiciones casi fijas.

Irreversibles
Los procesos de cambios irreversibles son esos que ocurren en un sólo sentido y que no pueden volver a la situación inicial.
Ejemplo:
El proceso de respiración
6O2 + C6H12O6 6H2O + 6CO2
x
Webgrafía
http://deconceptos.com/ciencias-naturales/materia#ixzz2DQm2guhP
http://es.wikipedia.org/wiki/Qu%C3%ADmica
http://hnncbiol.blogspot.com/2008/01/transformaciones-fsicas-y-qumicas-de-la.html
http://www.fullquimica.com/2011/11/definicion-de-reaccion-quimica.html
Lee todo en: Reacciones Químicas Reversibles | La Guía de Química
http://quimica.laguia2000.com/reacciones-quimicas/reacciones-quimicas-reversibles#ixzz2DQxl6MvF
https://www.codelcoeduca.cl/minisitios/docentes/pdf/naturales/3_naturales_NM1.pdf
http://www.rlabato.com/isp/qui/qui_fis_2011-011.pdf
Lee todo en: Factores que afectan a la velocidad de reacción | La Guía de Química
http://www.sistemadetutorias.com.ar/programa.html
Webgrafía
x