QUÍMICA
Aspectos analíticos de sustancias
Componente:
El Átomo
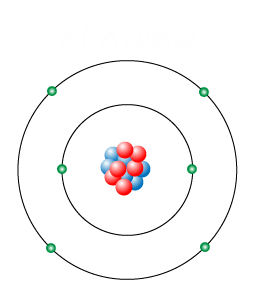
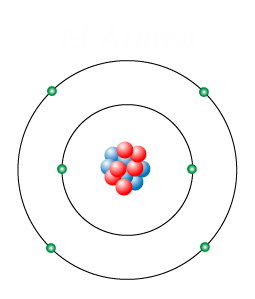
El átomo es la unidad de materia más pequeña de un elemento químico, que mantiene su identidad o sus propiedades y que no es posible dividir mediante procesos químicos.
El átomo está formado por un núcleo, compuesto a su vez por protones y neutrones, y por una corteza que lo rodea en la cual se encuentran los electrones, en igual número que los protones.
Número atómico (Z)
El número atómico, corresponde al número de cargas elementales positivas (protones) que contiene el núcleo de un átomo. Se representa con la letra Z. En un átomo eléctricamente neutro, el número de electrones orbitales es igual al número atómico.
Masa atómica (A)
La masa de un átomo en particular, corresponde a la suma de las masas de sus protones y neutrones. Se representa con la letra A.
Núcleo
El núcleo está ubicado en el centro del átomo; en él se encuentran los protones y los neutrones, los cuales constituyen prácticamente la totalidad de la masa del átomo, ya que la masa de los electrones, es despreciable, frente a estos. Desde el punto de vista eléctrico, el núcleo presenta carga positiva. El radio del núcleo, es unas 100.000 veces más pequeño que el radio del átomo.
Corteza
La corteza es la región que rodea al núcleo y que delimita el exterior del átomo; constituye casi totalmente el volumen del átomo, está ocupado únicamente por un número pequeño de partículas materiales, denominadas electrones. Desde el punto de vista eléctrico, la corteza posee carga negativa.
El Átomo
El átomo es la unidad de materia más pequeña de un elemento químico que mantiene su identidad o sus propiedades, y que no es posible dividir mediante procesos químicos.
El átomo está formado por un núcleo, compuesto a su vez por protones y neutrones, y por una corteza que lo rodea en la cual se encuentran los electrones, en igual número que los protones.
Electrón
Es la partícula elemental que constituye parte de cualquier átomo, fue descubierta en 1897 por J. J. Thomson. Los electrones de un átomo giran en torno a su núcleo, formando la denominada corteza electrónica. La masa del electrón es 1836 veces menor que la del protón y tiene carga negativa. En condiciones normales un átomo tiene el mismo número de protones que electrones, lo que convierte a los átomos en entidades eléctricamente neutras. Si un átomo capta o pierde electrones, se convierte en un ion.
Neutrón
partícula elemental que constituye parte del núcleo de los átomos. Fueron descubiertos en 1930 por dos físicos alemanes,Walter Bothe y Herbert Becker. La masa del neutrón es ligeramente superior a la del protón, pero el número de neutrones en el núcleo no determina las propiedades químicas del átomo, aunque sí su estabilidad frente a posibles procesos nucleares (fisión, fusión o emisión de radiactividad). Los neutrones carecen de carga eléctrica, y son inestables cuando se hallan fuera del núcleo, desintegrándose para dar un protón, un electrón y un antineutrino.
Electrón, partícula elemental que constituye parte de cualquier átomo, descubierta en 1897 por J. J. Thomson. Los electrones de un átomo giran en torno a su núcleo, formando la denominada corteza electrónica. La masa del electrón es 1836 veces menor que la del protón y tiene carga opuesta, es decir, negativa. En condiciones normales un átomo tiene el mismo número de protones que electrones, lo que convierte a los átomos en entidades eléctricamente neutras. Si un átomo capta o pierde electrones, se convierte en un ion.
Protón
descubierto por Ernest Rutherford a principios del siglo XX, el protón es una partícula elemental que constituye parte del núcleo de cualquier átomo. El número de protones en el núcleo atómico, denominado número atómico, es el que determina las propiedades químicas del átomo en cuestión. Los protones poseen carga eléctrica positiva y una masa 1.836 veces mayor de la de los electrones.
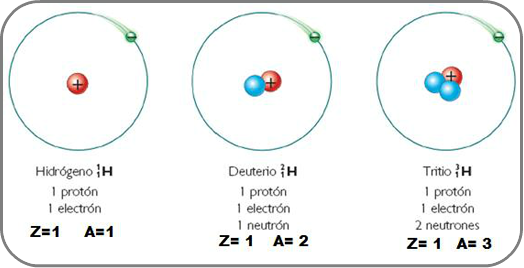
Isótopos
Los isótopos son las formas atómicas de un mismo elemento, que tienen número idéntico de protones (Z) en el núcleo, pero cuyo número de neutrones (N) es diferente. Los isótopos se distinguen en cuanto a la masa, aunque son de la misma naturaleza química.
Para representar un isótopo, hay que indicar el número másico (A) propio del isótopo y el número atómico (Z), colocados como índice y subíndice, respectivamente, a la izquierda del símbolo del elemento.