
QUÍMICA
Aspectos analíticos de mezclas
Componente:

-
Métodos de
separación
-
Filtración y
tamizado
-
Decantación y
centrifugación
-
Evaporación y
Magnetismo
-
Destilación
-
Webgrafía
Métodos de separación
En él se describen cualitativamente tanto los componentes de una mezcla, como las particularidades que permiten diferenciarla de otras. En lo cuantitativo se determinan las proporciones de los elementos que la conforman y se miden sus características distintivas.
En este componente se abordan las técnicas para el reconocimiento, la separación o la medición de mezclas, y las consideraciones teóricas en las que se fundamentan.
Webgrafía
http://es.scribd.com/doc/69542178/Mezclas-heterogeneas
http://iiquimica.blogspot.com/2006/07/mezclas-homogneas-y-heterogneas.html
http://es.wikipedia.org/wiki/Espuma
http://tplaboratorioquimico.blogspot.com/2008/12/sustancias-y-mezclas.html
http://html.rincondelvago.com/distincion-entre-mezclas-y-combinaciones-quimicas.html
http://www.slideshare.net/verosantiago/soluciones-qumicas-presentation#btnNext
http://www.javeriana.edu.co/Facultades/Ciencias/neurobioquimica/libros/celular/cromatografia.htm
http://www.quiminet.com/articulos/historia-de-la-cromatografia-de-gases-20851.htm
http://crhvscience.blogspot.com/2012/05/ii-trimestre-metodos-fisicos-de.html
Webgrafía
x
Homogéneas
Las mezclas homogéneas son aquellas que poseen características y propiedades semejantes en todas sus partes, sus componentes no son identificables a simple vista, es decir, se aprecia una sola fase física
Ejemplo:
El agua potable es una mezcla homogénea de agua (fase dispersante) y varias sales minerales (fase dispersa).
Mezclas
Una mezcla es una combinación física de dos o más sustancias puras, que poseen composición variable.
Reacción Química
Las mezclas son una asociación física de dos o más sustancias puras entre las que no existe reacción química. Al final de cualquier mezcla se seguirán teniendo las sustancias que se agregaron inicialmente en las mismas cantidades, no se obtendrán productos nuevos.
Sustancias
Una sustancia es una forma de materia que tiene una composición definida (constante) y propiedades características.
Ejemplos: El agua, el amoniaco, el azúcar (sacarosa), el oro, y el oxígeno
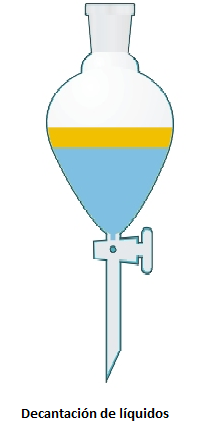
Decantación
La decantación es una técnica de separación que aprovecha la diferencia de densidades. Se aplica para separar una mezcla de líquidos o un sólido insoluble en un líquido.

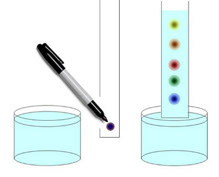
Cromatografía
La cromatografía es la separación física de dos o más compuestos, basada en la diferente distribución de dos fases, una de las cuales es la estacionaria y otra la móvil.
Cristalización
La cristalización es un método de purificación que permite separar los sólidos de mezclas homogéneas y heterogéneas, ya sean sólidas o líquidas. Este método se basa en la solubilidad que tienen los sólidos en los disolventes a diferentes temperaturas.

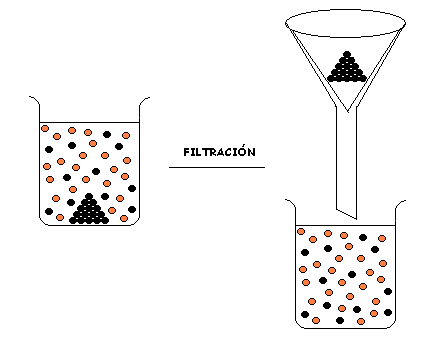
Filtración
El procedimiento de filtración consiste en retener partículas sólidas por medio de una barrera; la cual puede consistir en mallas, fibras, material poroso o un relleno sólido.
Evaporación
La evaporación, es un proceso que se usa para separar un sólido soluble de un líquido.
Ejemplo:
Cuando disolvemos sal (NaCl) en agua y queremos separarlos nuevamente, simplemente calentamos el agua hasta evaporarla y obtenemos la sal, ya que esta no se evapora.

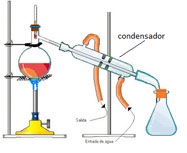
Destilación
La destilación es un proceso que se usa para separar un sólido soluble de un líquido o para separar dos líquidos solubles entre sí, para esto se calienta la mezcla líquida hasta que sus componentes más volátiles pasan a la fase de vapor o gas y, a continuación, se enfrían los vapores o gases en un tubo condensador, el cual como su nombre lo indica condensa los vapores y los vuelve líquidos nuevamente.
Centrifugación
La centrifugación, es un procedimiento que se utiliza cuando se quiere acelerar la sedimentación. Se coloca la mezcla dentro de una centrifuga, la cual tiene un movimiento de rotación constante y rápido, lográndose que las partículas de mayor densidad, se vayan al fondo y las más livianas queden en la parte superior.

Heterogéneas
Las mezclas heterogéneas son aquellas, cuyos componentes se pueden distinguir a simple vista, apreciándose más de una fase física.
Ejemplo: Agua con piedra, agua con aceite.
Soluciones
Las soluciones, son mezclas homogéneas que están formadas por dos o más sustancias puras.
Suspensiones
Las suspensiones están conformadas por una fase sólida insoluble en la fase dispersante líquida, por lo cual tiene un aspecto opaco. Las partículas dispersas son relativamente grandes.
Ejemplo: Arcilla, tinta china (negro de humo y agua), pinturas al agua, cemento.
Coloides
Los coloides o soles, son sistemas heterogéneos, en donde la fase dispersa está constituida por partículas llamadas micelas, las cuales se hallan en continuo movimiento, siguiendo trayectorias de zig-zag; a este fenómeno se le denomina Movimiento Browniano.
Aerosoles
Los aerosoles son suspensiones en gases. Si las partículas suspendidas son sólidas, entonces el aerosol se identifica con humo o polvo. Si por otro lado, las partículas suspendidas son líquidos, el aerosol se identifica con niebla.
Espumas
Una espuma es una suspensión de partículas gaseosas en un líquido. Las espumas son sistemas coloidales por la delgadez de las capas que rodean las burbujas de gas.
Son ejemplos de espumas, algunos alimentos como la crema batida y las espumas usadas para combatir incendios, que constan de burbujas de dióxido de carbono.
Emulsiones
Una emulsión es una mezcla de líquidos inmiscibles de manera más o menos homogénea. Un líquido (la fase dispersa) es dispersado en otro (la fase continua o fase dispersante).
Son ejemplos de emulsiones, la mantequilla, la margarina, y la leche.
Homogéneas
Reacción
química

Simple
vista
Decantación
Cromatografia
Cristalización
Filtración
Evaporación
Destilación
Centrifugación
Heterogéneas
Componentes
líquidos
Soluciones
Sus
componentes
simple
vista
Suspensiones
Coloides
Aerosol
Espuma
Emulsión
x
Combinaciones
