Destilación
Este método permite separar mezclas de dos o más líquidos miscibles, aprovechando los diferentes puntos de ebullición. Los líquidos como condición, deben de tener por lo menos 5º de diferencia en sus puntos de ebullición.
Destilación Simple
Destilación Fraccionada
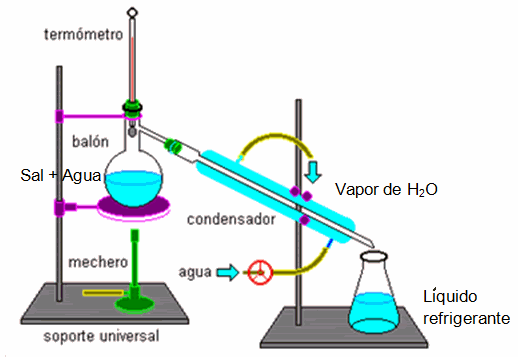
1. Destilación Simple:
Es empleada para separar aquellos líquidos cuyos puntos de ebullición difieren extraordinariamente (en más de 80°C aproximadamente) o para separar líquidos de sólidos no volátiles.
Por ejemplo, para separar la sal (NaCl) del agua, se calienta la mezcla homogénea; el agua se evapora y luego se condensa, y en el recipiente queda NaCl sólido, que no se evapora.
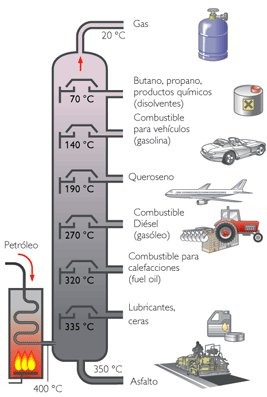
2. Destilación Fraccionada:
Es un proceso físico para separar líquidos miscibles en base a la diferencias de sus puntos de ebullición o condensación. Un ejemplo de destilación fraccionada, es la separación de los hidrocarburos del petróleo.